1)自愿加入本研究,并签署知情同意书;
2)年龄 18~80 周岁(包括边界值);
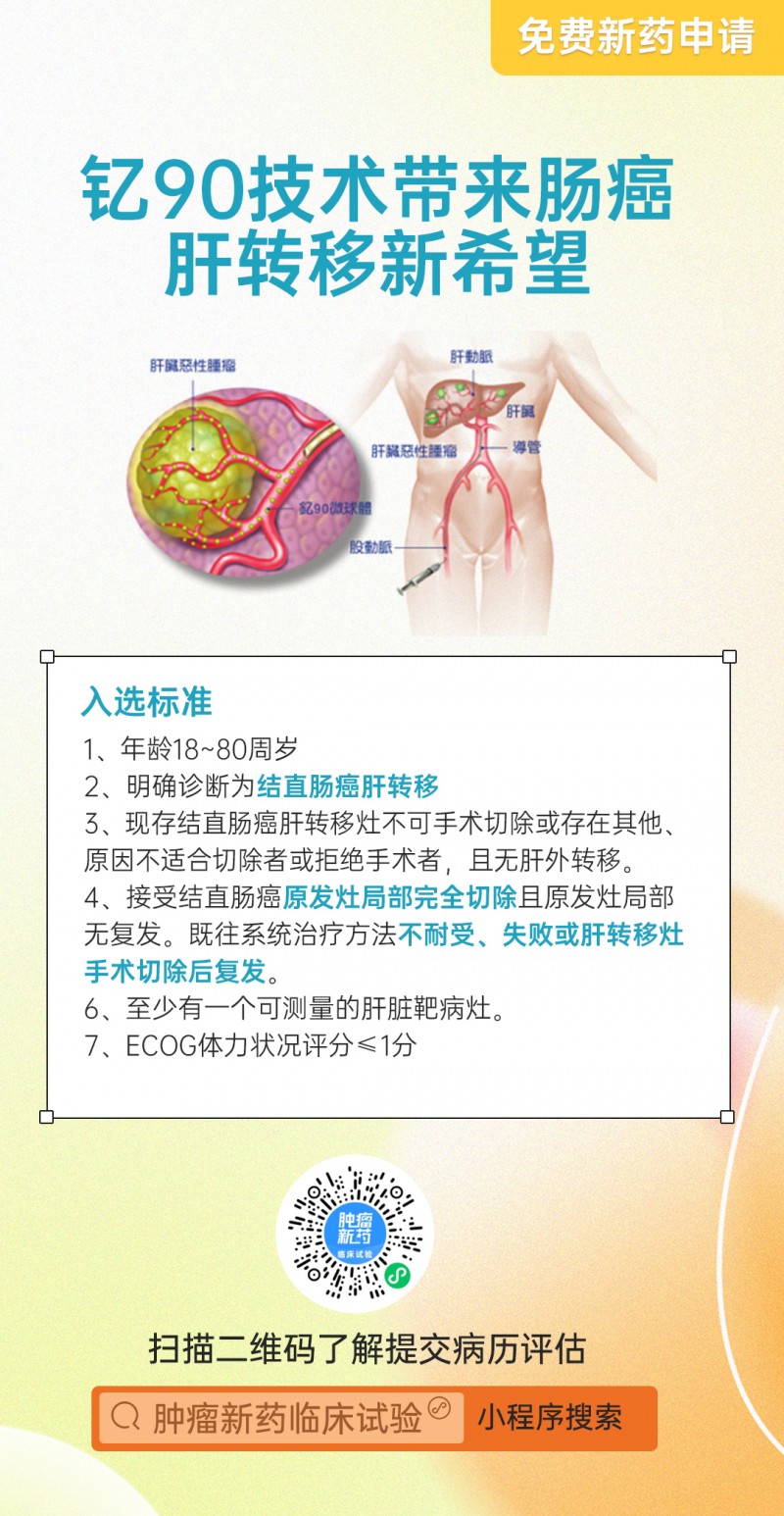
3)ECOG 体力状况评分≤1 分;
4)预计生存期≥3 m;
5)通过既往影像学或经病理和/或细胞学明确诊断为结直肠癌肝转移;
6)已成功接受结直肠癌原发灶局部完全切除且原发灶局部无复发;
7)既往抗肿瘤系统治疗方法不耐受、失败或肝转移灶手术切除后复发;
8)现存结直肠癌肝转移灶不可手术切除或研究者认为存在其他原因不适合切除者或拒绝手术者,且无肝外转移;
9)根据 RECIST1.1 标准,至少有一个可测量的肝脏靶病灶;
10)肿瘤总体积小于肝脏总体积的 50%;
11)Child-Pugh 评分≤7 分;
12)有足够的器官功能:
①血常规[14 天内未接受过输血或集落刺激因子(granulocyte /textarea/iy-stimulatingfactor,G-CSF)治疗]:中性粒细胞计数(absolute neutrophil count,ANC)≥1.5×10 9 /L;血小板计数(platelet counts,PLT)≥75×10 9 /L;血红蛋白(hemoglobin,HGB)≥90 g/L;
②肝功能:血清总胆红素(total bilirubin,TBIL)≤2 倍正常值上限(upper limit ofnormal,ULN);丙氨酸氨基转移酶(alanine transaminase,ALT)和天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)≤5.0 倍 ULN;碱性磷脂酶(alkalinephosphatase,ALP)≤2.5 倍 ULN;白蛋白>30 g/L;
③肾功能:肌酐(creatinine,Cr)1.5 倍 ULN;肌酐清除率(creatinine clearance,CCr)≥50 mL/min(根据 Cockcroft-Gault 公式计算);
④凝血功能:国际标准化比率(international normalized ratio,INR)、凝血酶原时间 ( prothrombin time , PT ) 和 活 化 部 分 凝 血 活 酶 时 间 ( activated partialthromboplastin time,APTT)≤1.5 倍 ULN。如受试者服用华法林或肝素进行抗凝治疗,需确定在停药或未用药时满足方案要求;
⑤心血管功能:心脏彩超检查:左室射血分数(left ventricular ejection fraction,LVEF)≥50%;
13)根据 CTCAE5.0 标准,既往系统抗癌治疗的所有不良事件恢复到基线或≤1 级[以下除外:既往抗癌治疗诱发的神经病变稳定(≤2 级),脱发];
14)育龄女性和男性必须同意在签署知情同意后、研究期间及试验结束后 6 m 内采取严格的有效的避孕措施,男性在此期间禁止捐献精子,育龄期的女性受试者筛选期及给药前 24 h 内复查的妊娠试验结果必须为阴性。
排除标准:
受试者符合下列任何一项排除标准,则不纳入本项研究:
1)既往有肝性脑病病史患者;
2)严重的肺功能不全(FEV1/FVC<50%或 FEV1<50%预计值或每分钟最大通气量(maximum volume per minute,MVV)<50 L/min)、明显的慢性阻塞性肺病或间质性肺炎的患者;3)锝[ 99mTc]聚合白蛋白(99mTc-MAA)动脉灌注显像显示肝肺分流百分数>10%或单次肺部辐射吸收剂量>30 Gy;
4)不可肝动脉插管者,如血管畸形、对造影剂过敏、对麻醉剂过敏等;
5)门静脉主干癌栓;
6)结直肠癌肝转移病灶既往接受过放射治疗者或经肝动脉栓塞者(接受经肝动脉非碘化油化疗栓塞的患者由研究者判断是否可入组);
7)上次抗肿瘤治疗(手术、化疗、免疫治疗、靶向治疗)距本试验药物给药前 4 w 以内者;
8)门脉高压症、中至重度单纯性腹水或难治性腹水或失代偿期肝硬化临床表现;
9)在试验药物给药之前 28 d 做过大手术或严重创伤;
10)距使用本试验药物前 1 m 内参加过其他干预性临床试验;
11)妊娠、哺乳期女性;
12)处于活动期或目前需系统治疗的严重感染;
13)人类免疫缺陷病毒抗体检查结果阳性者;
14)研究者判断,存在既往治疗的未解决的毒性并将继续存在,可能危及患者安全;
15)研究者认为受试者存在任何临床或实验室检查异常或其他原因不宜入选本研究。
二、研究产品:NRT6003 注射液(由钇[90Y]炭微球和辅料组成)
三、适应症:不可手术切除结直肠癌肝转移
四、试验分期:I/II 期
五、计划入组例数:60 例,计划完成入组时间,2023.6


























 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城